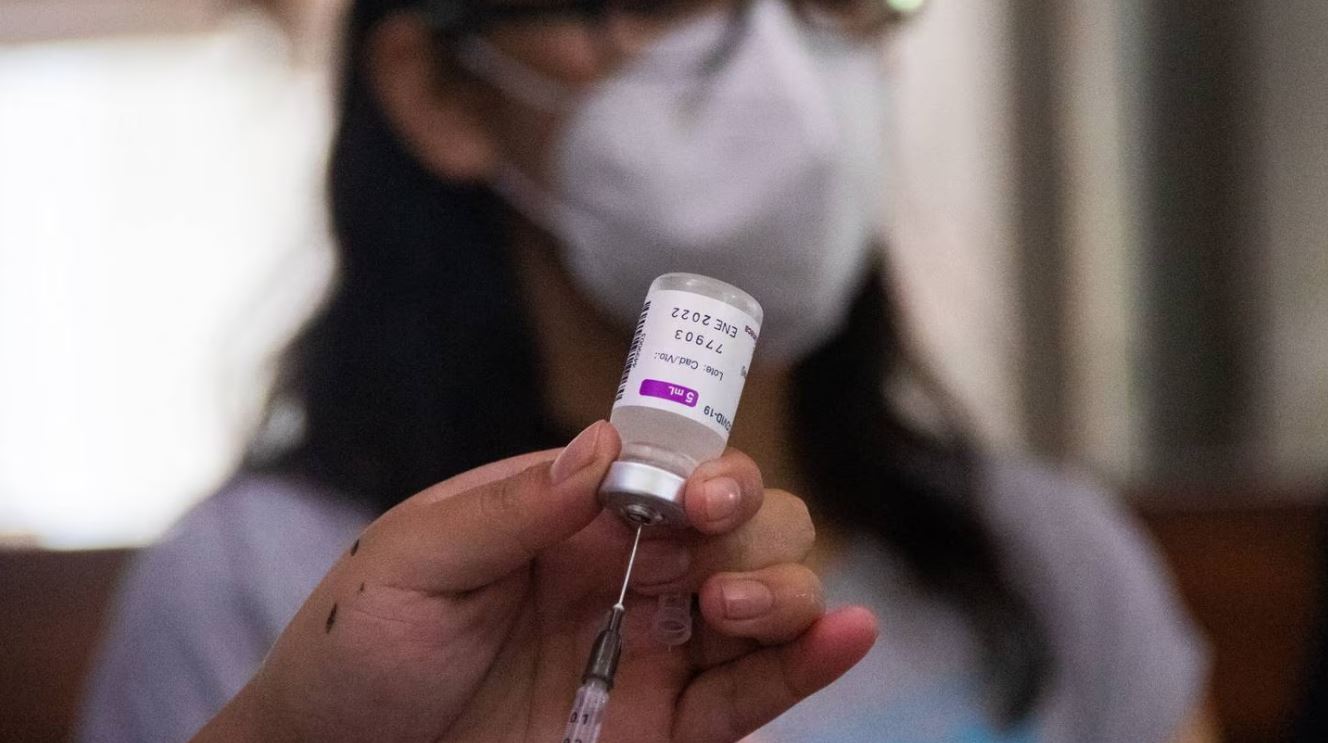
El Comité de Moléculas Nuevas (CMN) de la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) aprobó por unanimidad la solicitud para la obtención del registro sanitario de la vacuna monovalente Spikevax de la farmacéutica Moderna contra covid-19 y rechazó por mayoría de votos la solicitud para el inmunológico bivalente, al considerar que no se apega a las actuales recomendaciones de la Organización Mundial de la Salud (OMS).
En sesión pública, transmitida a través de sus redes sociales, los expertos integrantes del CMN, quienes expresaron su declaración de no conflicto de intereses y acuerdo de confidencialidad, señalaron que los datos presentados por Moderna cuentan con evidencia suficiente sobre la inmunogenicidad (capacidad para generar respuesta inmune) y seguridad de ambos biológicos.
Sin embargo, aclararon que considerando las recomendaciones recientes de la OMS, “es de mucho mayor relevancia el papel de la vacuna monovalente para la protección de la población, porque se apega a las recomendaciones y es de mayor eficacia para las cepas que circulan actualmente” en el mundo.
Por su parte, Moderna, reconoció que su vacuna bivalente combate cepas que ya no son tan relevantes actualmente, pero aseguró que como “concepto de refuerzo tiene valor”, en particular para los sectores de la población que no tuvieron acceso a la inmunización o que ya ha pasado mucho tiempo desde la serie primaria, por lo que “es capaz de generar capacidad neutralizantes del virus, sólo que no tan alta”.